Особенности влияния тонуса мышечной системы на нарушение энергетического баланса и способы его коррекции
1. В каждый момент времени в организме человека реализуется баланс между общим количеством (АТФ), синтезированным в клетках и израсходованным на различные нужды. Синтез АТФ, как известно, происходит внут-риклеточно, в митохондриях. И в этом смысле каждая клетка отдельного органа работает на собственные нужды, расходуя кислород и глюкозу.
Органы человека характеризуются различным удельным потреблением кислорода – пропорциональным энергетическому потреблению: Сердце = 440 кал/кг; Почки = 440 кал/кг; Мозг = 243 кал/кг; Печень = 198 кал/кг; Мышцы = 13 кал/кг; Жировая ткань = 4 кал/кг; Костная ткань = 2 кал/кг [1]. Для более наглядного представления об использовании энергетического ресурса организма полезно принять во внимание массу органа, Таблица 1.
На первый взгляд на вершине иерархии гомеостазов в потреблении энергетических ресурсов находится мозг. Однако данное распределение энергопотребления относится к стабильному нормальному состоянию здорового организма. Конкурентное расходование органами растворенного в плазме кислорода осуществляется в процессе диффузии кислорода из плазмы крови к клеткам органов. Основными параметрами в уравнении диффузии Фика:
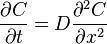
являются: градиент концентрации кислорода С, коэффициент диффузии D[см2сек-1]. Иммунная система является главным потребителем энергоресурсов. Расположение иммунокомпетентных клеток иммунной системы, а именно близость к растворенному в плазме крови кислороду, определяют их преимущество как потребителя кислорода по сравнению со всеми остальными органами. Развитие в организме воспалительных процессов в результате острых инфекций и /или аутоиммунных реакций, а также появление хронических воспалительных процессов может существенным образом изменить баланс потребителей энергоресурса организма. Развивающийся дефицит энергии, точнее дефицит кислорода, приводит к развитию анаэробных процессов, увеличению выработки активных форм кислорода (АФК) и, как следствие, повышению Ред/окс потенциала. Повышение Ред/окс потенциала приводит к существенному снижению транспортных возможностей эритроцитов и снижению парциального давлению кислорода в плазме крови [2]. Расходование кислорода происходит в соответствии с иерархией гомеостазов организма [3].
Недостаток кислорода по цепи обратной связи может привести к возбуждению (увеличение выброса возбуждающих нейротрансмиттеров), как средству увеличения дыхательной активности. Происходит смещение баланса глутамат – ГАМК эргических процессов в сторону возбуждения. Возбуждение вегетативной нервной системы может привести к гипертонусу мышц внутренних органов, желёз внутренней и внешней секреции, кровеносных и лимфатических сосудов. Происходит затруднение в циркуляции крови и возникающий дефицит кофакторов приводит к снижению ферментативной активности, нарушению процессов внутренних органов, желёз внутренней и внешней секреции, кровеносных и лимфатических сосудов, что ведет к дальнейшему нарастанию дефицита кислорода и что приводит к еще большему выбросу глутамата. Развивается Эксайтотоксичность – патологический процесс, ведущий к повреждению и гибели нервных клеток под воздействием нейромедиаторов, способных гиперактивировать ионотропные рецепторы глутамата. При этом излишнее поступление ионов кальция в клетку активирует ряд ферментов, разрушающих цитозольные структуры и приводит к запуску апоптоза клетки.
В качестве эксайтотоксинов может выступать L-глутамат. Процесс может играть определённую роль в патогенезе рассеянного склероза, болезни Альцгеймера, амиотрофического латерального склероза, болезни Паркинсона, болезни Гентингтона, а также в развитии глаукомной оптиконейропатии.
Таблица1. Энергопотребление органами.
| Масса, кг | Удельное потребление энергии, ккал · кг¹·сут¹ |
Мощность, Вт |
|
|---|---|---|---|
Печень |
1.8 |
200 |
17.4 |
Мозг |
1.4 |
240 |
16.2 |
Сердце |
0.33 |
440 |
7 |
Почки |
0.31 |
440 |
6.6 |
Скелетные мышцы |
28 |
14.5 |
19.8 |
Жировая ткань |
15 |
4.5 |
3.4 |
Другие ткани. |
23 |
12 |
13.6 |
2. Активность фермента пируватдегидрогеназы (ПДГ) является одним из определяющих факторов в цепи процессов синтеза АТФ. Пируватдегидрогеназный комплекс включает в себя три кофактора: Е1-пируватдегидрогеназа декарбоксилирующая. Кофактором является активная форма витамина В1. Е2-дигидролипоилацетилтрансфераза. Кофактором является витаминоподобное вещество – липоевая кислота, Коферментом является активная форма пантотеновой кислоты. Е3-дигидролипоилдегидрогеназа. Кофактором является флавинадениндинуклеотид (ФАД) – активная форма витамина В2. Коферментом является активная форма витамина РР – никотинамидадениндинуклеотид (НАД+).
Использование различных форм витаминных препаратов, как правило, в состоянии создать достаточную концентрацию витаминов в плазме крови. Однако, эффективность работы ферментов в органах и мышцах как бы не реагирует на большие и сверх большие дозы витаминов. Отсюда и распространённое заблуждение: «витамины не попадают в кровь». На этом посыле создаются специальные формы витаминов для достижения сверх концентраций в плазме крови.
Любопытные данные были опубликованы в "Ланцете", результаты очень большого исследования Heart Protection Study. В нем участвовали более 20 тысяч человек с высоким риском сердечно-сосудистых заболеваний.
У них изучались защитные эффекты все тех же антиоксидантов – бета-каротина и витаминов С и Е. В течение пятилетнего наблюдения препараты ничуть не препятствовали развитию сердечных приступов, инсультов и различных раковых заболеваний. При этом содержание самих витаминов в крови возрастало.
Результаты, полученные при изучении влияния комбинированного действия витаминов группы В и синтетического агониста ГАМК – ергических рецепторов центров никотиноилгамма-аминомасляной кислоты проливают свет на истинные причины возможного недостатка витаминов группы В в тканях и органах [4]. Таблица 2. Основной задачей проведенного исследования явилось изучение возможности применения препарата никотиноил-гамма-аминомасляной кислоты для изменения активности пируватдегидрогеназы (ПДГ).
Из приведенных выше данных видно, что увеличение активности ПДГ происходит при совместном использовании агониста тормозных рецепторов и витамина В1. Влияние тормозных (расслабляющих) эффектов наиболее выражено для паренхиматозных органов.
Превалирование процессов возбуждения в вегетативной нервной системе над процессами торможения приводит к гипертонусу гладкой мускулатуры стромы паренхиматозных органов. Поскольку строма, помимо опорной функций, выполняет трофическую функцию, гипертонус приводит к затруднению проводимости расположенных в ней кровеносных, лимфатических сосудов и нервов.
Наблюдаемый синергизм действия никотиноил-гамма-аминомасляной кислоты и витаминов группы В может быть объяснён тормозным влиянием синтетического агониста Никотиноил-гамма-аминомасляная кислоты на вегетативную нервную систему.
Показательно применение препаратов расслабляющих мускулатуру при лечении гиперплазии предстательной железы. Строма предстательной железы составляет 60% гиперплазированной простаты. Снятие гипертонуса гладкой мускулатуры стромы устраняется динамический компонент инфравезикальной обструкции[5]. Изменение соотношения лактат/пируват, определяющееся активностью ПДГ, считается маркером оксидантного стресса и гипоксии, оно коррелирует с цитоплазматическим уровнем NADH:NAD+ и может быть использовано как мера окислительно-восстановительного потенциала клетки. [6]
3. Препарат «Гитагамп» зарегистрирован на территории РФ (Р №001526/01).
Гитагамп (капсулы) – оригинальный отечественный препарат. В его состав входят: тиамина хлорид – 0,025 г; рибофлавин – 0,025 г; пиридоксин – 0,025 г; никотиновая кислота – 0,025 г; кальция пантотенат – 0,025 г; кислота фолиевая – 0,00005г; цианкобаламин – 0,000025 г; никотиноил-гамма-аминобутират натрия 0,05г.
Препарат, разработан для «терапии прикрытия», а именно для снижения нежелательных побочных эффектов, возникающих при приеме сильнодействующих средств.
В России побочные действия лекарственных средств или последствия от их неправильного приема становятся причиной госпитализации в 17-18% случаев от общего числа больных. Этот же фактор в развитых странах мира стоит на 4-6-м месте в ряду основных причин смертности населения. Необходимость учитывать возможность таких осложнений привела к возникновению в фармакологии относительно нового понятия – «терапия прикрытия» (add-back therapy). Такой метод борьбы с побочными реакциями лекарственных средств предусматривает назначение препаратов, снимающих нежелательные симптомы заранее, до начала курсового назначения основных препаратов. Сегодня в России появился первый препарат, специально разработанный для использования в терапии прикрытия. Этим препаратом является Гитагамп, эффективность которого в неврологической, психиатрической и наркологической практике была доказана в ходе нескольких клинических испытаний на территории Российской Федерации в 2003-2005 годах. Применение Гитагампа основывалось на предположении, что препарат сможет снижать побочные эффекты и приводить к более быстрому снижению симптомов основного заболевания. Эти предположения получили блестящие клинические подтверждения. Было показано, что на фоне Гитагампа быстрее происходит купирование компонентов субдепрессий, возникающих, например, при лечении хронического алкоголизма галоперидолом и циклодолом или амитриптилином. Аналогично было показано, что аффективные, психические и соматические компоненты субдепрессий у больных в основных группах проходят быстрее и чаще, по сравнению с контрольной группой, также при использовании Гитагампа вместе с блокаторами опиатных рецепторов при лечении больных героиновой наркоманией. Терапия прикрытия должна применяться для предупреждения субдепрессивных состояний, возникающих при длительном курсовом приеме других сильнодействующих средств, например, при лечении туберкулеза, при лечении гепатита С интерфероном или при использовании такого известного антибиотика как кларитромицин, прием которого часто сопровождается депрессивными явлениями.
Заключение
Уникальная эффективность препарата Гитагамп является результатом сочетания действия синтетического агониста ГАМК – ергичес-ких рецепторов и витаминов группы В.
За счет расслабления мускулатуры (стромы) достигается эффективная доставка компонентов плазмы к органам и тканям. Возрастает активность витамин зависимых ферментов. Происходит, в частности, увеличение активности пируватдегидрогеназы и увеличение скорости синтеза Аденозинтрифосфата (АТФ), что существенным образом улучшает самочувствие пациента, а также может препятствовать развитию неврологических заболеваний.
Список литературы
1. In:Kinney JM, TuckerHN, eds. «Energy metabolism: tissue determinants and cellular corollaries.» New York, NY: Raven Press, 1992:61–80.2. И.Г. Гитлин, Е.З. Гольдберг «Неврология, психиатрия и оксидативный стресс. Защитные свойства Гитагамп — Рутин Железо». Журнал международной медицины. Неврология. Психиатрия / 2013 / Номер 2 (3), стр101-106.
3. Кукес В.Г., Гитлин И.Г. «Персонализированная медицина и окислительно восстановительный гомеостаз.», Лекарственные препараты и рациональная фармакотерапия, №2, 2014, стр 23-25
4. Л Л .М . Карпов , В .Г .Савчук , А .В .Запорожченко , Т .В . Бахтогареева , О .В . Сторчило , Л .А . Медаковская. «Изучение действия препарата никотиноил гамма-амино-масляной кислоты и витаминов группы В на некоторые биохимические и физиологические процессы в организме экспериментальных животных». УДК 615.214.31.03:616-008.93-092.9 Одесский госуниверситет им. И.И. Мечникова.
5. /Лоран О.Б" Пушкарь Д.Ю., Раснер П.И. Патогенетические основы медикаментозной терапии симптоматической доброкачественной гиперплазии простаты альфа-адреноблокаторамн. И Лечащий врач. №9. 2001.
6. CHRISTINE B. and all «Pyruvate dehydrogenase complex deficiency: four neurological phenotypes with differing pathogenesis». Developmental Medicine & Child Neurology Volume 52, Issue 2, Article first published online: 1 DEC 2009


